تفاوت اسید نیتریک غلیظ و رقیق چیست؟
اسید نیتریک (Nitric Acid) با فرمول شیمیایی HNO₃ یکی از مهمترین اسیدهای معدنی در صنایع شیمیایی، کشاورزی، نظامی و آزمایشگاهی است. اما نکتهای که بسیاری از مصرفکنندگان صنعتی و حتی دانشجویان شیمی با آن مواجهاند، تفاوت اسید نیتریک غلیظ و رقیق و تأثیر آن بر واکنشها، ایمنی و کاربردهای صنعتی است.
در این مقاله بهصورت جامع بررسی میکنیم:
- اسید نیتریک غلیظ و رقیق چیستند؟
- تفاوت آنها از نظر شیمیایی، واکنشپذیری و کاربرد چیست؟
- هرکدام در چه شرایطی استفاده میشوند؟
اسید نیتریک چیست؟
اسید نیتریک (Nitric Acid) یک اسید معدنی قوی با فرمول HNO₃ است که:
- در آب بهطور کامل یونیزه میشود.
- خاصیت خورندگی بالایی دارد.
- یک اکسیدکننده قوی محسوب میشود.
- ساختار مولکولی خاص اسید نیتریک باعث شده است که علاوه بر خاصیت اسیدی، در بسیاری از واکنشها نقش عامل اکسیدکننده را نیز ایفا کند.
ویژگی شیمیایی اسید نیتریک غلیظ چیست؟
اسید نیتریک غلیظ به محلولی از HNO₃ گفته میشود که معمولا:
- غلظتی بیش از ۶۸ درصد دارد.
- رنگ آن زرد تا زرد مایل به قهوهای است.
- حاوی مقادیر حلشدهای از دیاکسید نیتروژن (NO₂) است.
- ویژگیهای اسید نیتریک غلیظ
- قدرت اکسیدکنندگی بسیار بالا
- واکنشپذیری شدید
- تولید بخار سمی NO₂
- خورندگی شدید برای پوست، فلزات و مواد آلی
- قابلیت پسیو کردن برخی فلزات
ویژگی شیمیایی اسید نیتریک رقیق چیست؟
اسید نیتریک رقیق محلولی از HNO₃ با درصد پایینتر آب است که معمولا:
| 1 |
غلظتی بین ۵ تا ۲۰ درصد |
| 2 |
ظاهری شفاف و بدون دود |
| 3 |
واکنشهایی قابلکنترلتر دارد |
| 4 |
ویژگی اسید نیتریک رقیق |
| 5 |
خاصیت اسیدی قوی |
| 6 |
اکسید کنندگی کمتر نسبت به نوع غلیظ |
| 7 |
ایمنتر برای مصارف آزمایشگاهی |
| 8 |
واکنش ملایم تر با فلزات |
تفاوت اصلی اسید نیتریک غلیظ و رقیق
1. قدرت اکسیدکنندگی اسید نیتریک
یکی از اصلیترین تفاوتها، قدرت اکسیدکنندگی است:
- اسید نیتریک غلیظ: اکسیدکننده بسیار قوی
- اسید نیتریک رقیق: اکسیدکننده ضعیفتر
- همین تفاوت باعث اختلاف اساسی در محصولات واکنش میشود.
واکنش اسید نیتریک غلیظ و رقیق با فلزات
-
اسید نیتریک غلیظ با فلزات
اسید نیتریک غلیظ هنگام تماس با فلزاتی مانند مس، باعث واکنش شدید و تولید بخار قهوهای NO₂ میشود.
-
اسید نیتریک رقیق با فلزات
در حالت رقیق، واکنش ملایمتر است و محصول گازی متفاوتی تولید میشود.
3Cu + 8HNO₃ (dilute) → 3Cu(NO₃)₂ + 2NO + 4H₂O
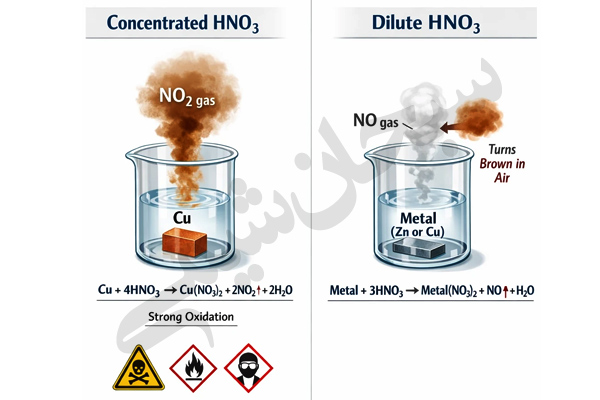
✅ نتیجه:
- تولید گاز NO (بیرنگ)
- واکنش کنترلشدهتر
- ایمنی بالاتر
- بخار NO₂ در اسید نیتریک
- بخار NO₂ یکی از شاخصترین تفاوتهای اسید نیتریک غلیظ و رقیق است.
✅ در اسید نیتریک غلیظ:
بخار قهوهای و سمی NO₂
خطر استنشاق بالا
✅ در اسید نیتریک رقیق:
تولید بسیار کم یا نامحسوس
NO₂ گازی بسیار سمی است که استنشاق آن میتواند منجر به آسیبهای ریوی شدید شود.
واکنش شیمیایی ترکیب اسید نیتریک غلیظ با آهن و آلومینیوم
1- آهن و آلومینیوم را پسیو (غیرفعال) میکند.
2- لایه محافظ اکسیدی تشکیل میدهد.
واکنش شیمیایی ترکیب اسید نیتریک غلیظ با آهن و آلومینیوم
2- موجب حل شدن تدریجی فلز میشود.
3- این ویژگی در صنایع فلزی اهمیت زیادی دارد.

کاربرد اسید نیتریک غلیظ در صنایع چیست؟
کاربرد اسید نیتریک غلیظ معمولا در فرآیندهایی است که نیاز به واکنش شدید یا اکسیدکنندگی بالا دارند:
- تولید مواد منفجره (TNT، RDX)
- نیتراسیون ترکیبات آلی
- تولید نیتراتهای صنعتی
- صنایع نظامی و پیشرانهها
- فرآوری فلزات خاص
- صنایع شیمیایی سنگین
- کاربرد اسید نیتریک رقیق
کاربرد اسید نیتریک رقیق در صنایع چیست؟
- آزمایشگاههای شیمی
- شستشو و تمیزکاری شیشهآلات
- اچکاری ملایم فلزات
- تولید نمکهای نیتراتی در مقیاس کوچک
- تحقیقات دانشگاهی و آموزشی
جدول تفاوت اسید نیتریک غلیظ با اسید نیتریک رقیق
| ویژگی |
اسید نیتریک غلیظ |
اسید نیتریک رقیق |
| درصد معمول |
65 – 68 (درصد) |
10–55 (درصد) |
| قدرت اکسیدکنندگی |
بسیار قوی |
متوسط |
| واکنش با فلزات |
تولید NO₂ قهوهای |
تولید NO بیرنگ |
| خطرات |
بسیار خورنده و خطرناک |
ایمنتر ولی همچنان خورنده |
| کاربرد اصلی |
صنایع، آزمایشگاه |
شستشو، تنظیم pH |
نکات ایمنی و خطرات اسید نیتریک غلیظ چیست؟
اسید نیتریک غلیظ یکی از خطرناکترین اسیدهای معدنی محسوب میشود:
| 1 |
سوختگی شدید پوست
|
| 2 |
تخریب چشم و بافتها
|
| 3 |
تولید NO₂ سمی
|
| 4 |
خطر انفجار در تماس با مواد آلی
|
| 5 |
نیاز به تهویه و تجهیزات ایمنی کامل
|
✅ استفاده صنعتی آن فقط با رعایت کامل استانداردهای ایمنی مجاز است.
خلوص استاندارد اسید نیتریک در کاربردهای مختلف
درصد اسید نیتریک صنعتی بسته به کاربرد متفاوت است:
| 1 |
کاربردهای عمومی صنعتی |
55 درصد |
| 2 |
صنعتی سنگین |
65 - 68 درصد |
| 3 |
کاربردهای خاص و نیتراسیون |
68 درصد |
✅ انتخاب درصد مناسب، تاثیر مستقیم روی ایمنی، کیفیت واکنش و هزینه دارد.
سوالات متداول
✍️ آیا اسید نیتریک غلیظ خطرناکتر است؟
بله، به دلیل خاصیت اکسیدکنندگی بالا
✍️ آیا میتوان اسید نیتریک غلیظ را رقیق کرد؟
بله، ولی فقط با افزودن اسید به آب، نه برعکس
✍️ اسید نیتریک 55٪ غلیظ محسوب میشود؟
خیر، در دسته اسید نیتریک رقیق قرار میگیرد.
جمعبندی نهایی
تفاوت اسید نیتریک غلیظ و رقیق تنها در میزان آب نیست، بلکه به:
- قدرت اکسیدکنندگی
- نوع واکنش با فلزات
- تولید بخار NO₂
- سطح خطر
اگر به واکنشهای قوی و صنعتی نیاز دارید، اسید نیتریک غلیظ مناسب است. اما برای کارهای کنترلشده، آزمایشگاهی و ایمنتر، اسید نیتریک رقیق انتخاب بهتری خواهد بود.
📚 پیشنهاد مطالعه: صفر تا صد ساختار شیمیایی اسید نیتریک